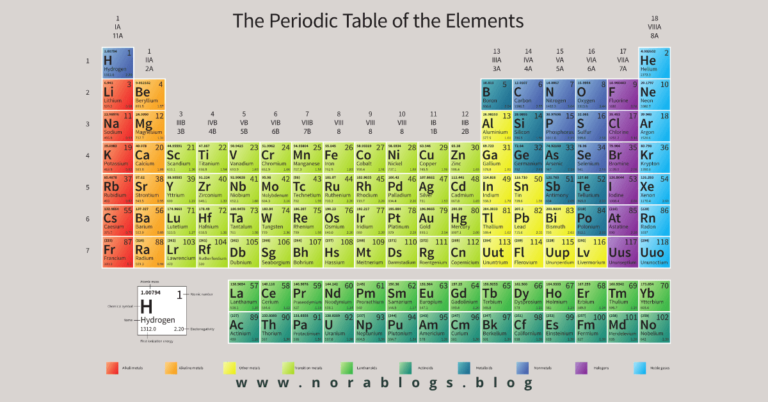
يرتب الجدول الدوري للعناصر الكيميائية العناصر الكيميائية في صفوف وأعمدة، وإنه رمز تنظيمي للكيمياء ويستخدم على نطاق واسع في الفيزياء والعلوم الأخرى، ويتم تدريسه في معظم جامعات العلوم.
تطور الجدول الدوري:
كان الجدول الدوري الأول الذي تم قبوله بشكل عام هو جدول الكيميائي الروسي دميتري منديليف في عام 1869.
لقد صاغ القانون الدوري على أنه اعتماد للخصائص الكيميائية على الكتلة الذرية. نظرًا لعدم معرفة جميع العناصر في ذلك الوقت، كانت هناك فجوات في جدوله الدوري، واستخدم Mendeleev بنجاح القانون الدوري للتنبؤ ببعض خصائص بعض العناصر المفقودة، وتم الاعتراف بالقانون الدوري باعتباره اكتشافًا أساسيًا في أواخر القرن التاسع عشر.
تم شرحه في وقت مبكر من القرن العشرين، مع اكتشاف الأعداد الذرية والعمل الرائد المصاحب في ميكانيكا الكم، كلا الفكرتين تعملان على إلقاء الضوء على البنية الداخلية للذرة.
تم التوصل إلى شكل حديث معروف للجدول في عام 1945 مع اكتشاف جلين تي سيبورج أن الأكتينيدات كانت في الواقع عناصر كتلة f بدلاً من عناصر d-block. الجدول الدوري والقانون هما الآن جزء أساسي لا غنى عنه في الكيمياء الحديثة.
يستمر الجدول الدوري في التطور مع تقدم العلم، حيث أن في الطبيعة، توجد فقط عناصر تصل إلى العدد الذري 94؛ للمضي قدمًا، كان من الضروري تجميع عناصر جديدة في المختبر.
اليوم، في حين أن جميع العناصر الـ 118 الأولى معروفة، وبالتالي إكمال الصفوف السبعة الأولى من الجدول، لا تزال هناك حاجة للتوصيف الكيميائي لأثقل العناصر لتأكيد تطابق خصائصها مع مواقعها.
لم يُعرف بعد إلى أي مدى سيتجاوز الجدول هذه الصفوف السبعة وما إذا كانت أنماط الجزء المعروف من الجدول ستستمر في هذه المنطقة غير المعروفة.
تستمر بعض المناقشات العلمية أيضًا حول ما إذا كانت بعض العناصر موضوعة بشكل صحيح في جدول اليوم.
توجد العديد من التمثيلات البديلة للقانون الدوري، وهناك بعض النقاش حول ما إذا كان هناك شكل أمثل للجدول الدوري.
ترتيب الجدول الدوري للعناصر:
ينقسم الجدول إلى أربع مناطق مستطيلة تقريبًا تسمى الكتل. تميل العناصر في نفس المجموعة إلى إظهار خصائص كيميائية متشابهة.
الاتجاهات الرأسية والأفقية والقطرية تميز الجدول الدوري، يزيد الحرف المعدني من النزول إلى مجموعة وينخفض من اليسار إلى اليمين عبر فترة، ويزيد الحرف غير المعدني من أسفل يسار الجدول الدوري إلى أعلى اليمين.
كل عنصر كيميائي له رقم ذري فريد (Z) يمثل عدد البروتونات في نواته، وتحتوي معظم العناصر
على نظائر متعددة، وهي متغيرات لها نفس عدد البروتونات ولكن بأعداد مختلفة من النيوترونات.
على سبيل المثال، يحتوي الكربون على ثلاثة نظائر طبيعية:
تحتوي كل ذراته على ستة بروتونات ومعظمها يحتوي على ستة نيوترونات أيضًا، ولكن حوالي واحد بالمائة بها سبعة نيوترونات، وجزء صغير جدًا به ثمانية نيوترونات.
لا يتم فصل النظائر مطلقًا في الجدول الدوري؛ يتم تجميعها دائمًا معًا تحت عنصر واحد. عندما يتم عرض الكتلة الذرية، فإنها عادة ما تكون المتوسط المرجح للنظائر التي تحدث بشكل طبيعي؛ ولكن في حالة عدم وجود أي منها، تظهر كتلة النظير الأكثر استقرارًا عادةً بين قوسين.
الترتيب في الجدول الدوري القياسي:
في الجدول الدوري القياسي، يتم سرد العناصر بترتيب زيادة العدد الذري Z. ويبدأ صف جديد (فترة) عندما يكون لإلكترون جديد غلاف إلكترون جديد. يتم تحديد الأعمدة (المجموعات) من خلال التكوين الإلكتروني للذرة؛ العناصر التي لها نفس عدد الإلكترونات في قشرة فرعية معينة تقع في نفس الأعمدة (على سبيل المثال، يوجد الأكسجين والسيلينيوم في نفس العمود لأن كلاهما يحتوي على أربعة إلكترونات في الجزء الفرعي p الخارجي).
العناصر ذات الخصائص الكيميائية المتشابهة تقع عمومًا في نفس المجموعة في الجدول الدوري، على الرغم من أنها في الكتلة f، وإلى حد ما في الكتلة d، تميل العناصر في نفس الفترة إلى خصائص مماثلة أيضًا. وبالتالي، فمن السهل نسبيًا التنبؤ بالخصائص الكيميائية لعنصر ما إذا كان المرء يعرف خصائص العناصر من حوله.
أول 94 عنصرًا تحدث بشكل طبيعي؛ أما الـ 24 المتبقية، من الأميريسيوم إلى الأوجانيسون (95-118)، فتحدث فقط عند تصنيعها في المختبرات، ومن بين 94 عنصرًا طبيعيًا، هناك 83 عنصرًا بدائيًا و 11 عنصرًا يحدث فقط في سلاسل الاضمحلال للعناصر البدائية، ولم يلاحظ أي عنصر أثقل من أينشتينيوم (العنصر 99) في الكميات العيانية في شكله النقي، ولا الأستاتين (العنصر 85) ؛ تم تصوير الفرانسيوم (العنصر 87) فقط في شكل ضوء ينبعث من كميات مجهرية (300000 ذرة).
أسماء وأرقام المجموعات:
– يتم ترقيم المجموعات رقميًا من 1 إلى 18 من العمود الموجود في أقصى اليسار (الفلزات القلوية) إلى العمود الموجود في أقصى اليمين (الغازات النبيلة). يتم تجاهل مجموعات الكتلة f في هذا الترقيم.
يمكن أيضًا تسمية المجموعات حسب العنصر الأول، على سبيل المثال “مجموعة سكانديوم” للمجموعة 3.
– في السابق، كانت المجموعات تُعرف بالأرقام الرومانية. في أمريكا، كانت الأرقام الرومانية متبوعة إما بـ “A” إذا كانت المجموعة في s- أو p-block ، أو “B” إذا كانت المجموعة في d-block.
– تتوافق الأرقام الرومانية المستخدمة مع الرقم الأخير من اصطلاح التسمية اليوم
(على سبيل المثال، كانت عناصر المجموعة 4 هي المجموعة IVB، وكانت المجموعة 14 عنصرًا من المجموعة IVA).
– في أوروبا، كانت الحروف متشابهة، باستثناء استخدام الحرف “A”
إذا كانت المجموعة قبل المجموعة 10، واستخدم الحرف “B” للمجموعات بما في ذلك المجموعة 10.
بالإضافة إلى ذلك، كانت المجموعات 8 و 9 و 10 تعامل على أنها مجموعة واحدة ثلاثية الحجم،
تعرف مجتمعة في كلا الترميزين بالمجموعة الثامنة.
– في عام 1988، تم وضع نظام التسمية الجديد IUPAC (الاتحاد الدولي للكيمياء البحتة والتطبيقية)
(1–18) قيد الاستخدام، وتم إهمال أسماء المجموعات القديمة (I-VIII).
استخدام الجدول الدوري للعناصر الكيميائية:
يمكن استخدام الجدول الدوري لمعرفة عدد كبير من المعلومات الخاصة بالعناصر؛ كرمز العنصر، وعدده الذري، وكتلته الذرية، وغيرها من المعلومات الأخرى، ويكون كل عنصر من عناصر الجدول الدوري موجوداً ضمن مربع صغير في الجدول، وفيما يأتي بعض المعلومات التي يمكن معرفتها عبر كل مربع خاص بالعنصر:
رمز العنصر:
هو اختصار لاسم العنصر الذي يشير إليه، وقد تُشير بعض الرموز إلى الأسماء اللاتينية القديمة
لأسماء العناصر؛ كاختصار رمز الفضة (Ag) الذي يشير إلى اسم العنصر القديم، وهو (Argentum).
العدد الذري:
هو عدد البروتونات التي تحتويها ذرة واحدة من ذرات العنصر، ويتركز الاهتمام بالبروتونات
لأنّها تميّز العنصر عن الآخر، في حين أنّ تغير عدد الإلكترونات والنيترونات في عنصر معين لا يُغير نوعه.
الكتلة الذرية:
هي متوسط كتلة العنصر بالنسبة لنظائره.
اسم العنصر:
هو الاسم العلمي للعنصر، حيث تحتوي العديد من الجداول الدورية على العناصر جنباً إلى جنب مع رموزها.
وبذلك، يعتبر الجدول الدوري الحديث من أهم الأدوات التى يمكن الاستفادة منها عند الحاجة لترتيب العناصر الكيميائية، أو الحصول على معلومات عن العناصر الكيميائية الموجودة بالعالم.